Gianluca Svegliati Baroni, Marta Mazzetti, Alesio Ortolani
Dipartimento di Scienze Cliniche e Molecolari, Sezione Gastroenterologia
Facoltà di Medicina e Chirurgia, Università Politecnica delle Marche
Le malattie epatiche presentano un ampio spettro di gravità e di sintomatologia la cui diagnosi si avvale di un insieme di esami di laboratorio e strumentali. Nessun esame da solo è in grado di giungere ad una diagnosi, ma è l’insieme dei test clinico-strumentali che permette la definizione del quadro clinico. Allo stesso modo anche il follow-up delle patologie epatiche si avvale della combinazione degli esami di laboratorio e dell’imaging, che si devono unire all’ esperienza clinica ed all’ utilizzo delle linee guida internazionali. Di seguito verrà approfondito il ruolo degli esami di laboratorio, degli esami strumentali e della biopsia epatica. Ne è passato di tempo da quando il fegato degli animali veniva utilizzato per predire il futuro.
Laboratorio
Gli esami ematochimici sono un efficace metodo sia per la diagnosi della funzionalità epatica che per il monitoraggio e la valutazione della risposta terapeutica.
I test più utilizzati includono le tramsaminasi (alanina aminotransferasi- ALT e aspartato aminotransferasi- AST), come indici di citolisi epatica; la fosfatasi alcalina (ALP), la gamma-glutamiltransferasi (GGT) e la bilirubinemia come indicatori della funzione bilio-escretrice; il tempo di protrombina/INR e l’albumina sierica come indici indiretti di funzionalità epatica. Una volta differenziati i principali quadri clinici (ostruzione del tratto biliare, danno acuto epatocellulare, malattia epatica cronica) è necessario eseguire ulteriori esami per individuarne le possibili cause, fra cui i markers delle epatiti virali e la determinazione di autoanticorpi per le patologie autoimmuni.
Transaminasi
Le transaminasi sono enzimi che appartengono alla classe delle trasferasi e catalizzano la reazione di trasferimento di un gruppo amminico da un aminoacido ad un chetoacido.
L’aspartato aminotrasferasi (AST, detta anche transaminasi glutammico ossalacetica, GOT) è un enzima aspecifico, riscontrabile anche nel cuore, nel muscolo scheletrico e nel rene. Se ne conoscono due frazioni, una citoplasmatica (AST I, presente al 60%) e una mitocondriale (AST II, presente al 40%).
L’Alanina aminotrasferasi (ALT, detta anche transaminasi glutammico piruvica (GPT) è un enzima esclusivamente citoplasmatico, è presente soprattutto nel fegato e nel rene e meno nel cuore e nel muscolo scheletrico, di conseguenza è più specifico rispetto alle AST per il fegato. Cause epatiche più comuni di ipertransaminasemia sono la steatoepatite non alcolica, le epatiti virali, l’epatopatia esotossica, l’epatite autoimmune e le epatopatie da accumulo (Morbo di Wilson ed emocromatosi) e da farmaci.
L’abuso etilico è una causa frequente di incremento della AST ed è un cofattore di danno epatico per le epatopatie metaboliche e virali. Occorre sempre sospettare un abuso etilico in presenza di un rapporto AST/ALT maggiore di 2 associato ad un aumento delle GGT. Altre cause di ipertransaminasemia sono la celiachia, le epatopatie infiltrative (amiloidosi), le patologie granulomatose (sarcoidosi, tubercolosi), le tesaurismosi (glicogenosi e glicosfingolipidosi) e le infiltrazioni neoplastiche del fegato.
Cause extra epatiche di ipertransaminasemia sono infine le malattie muscolari, l’emolisi e l’infarto del miocardio e l’esercizio fisico intenso.
Fosfatasi alcalina
Le fosfatasi alcaline sono prodotte da geni diversi e classificate in FA tessuto-specifica (correlato al metabolismo osseo e alle lesioni epato-biliari), FA intestinale (non è un marcatore specifico, in quanto fisiologicamente aumenta dopo i pasti ed è metabolizzata più velocemente degli altri due isoenzimi e per questo ha una bassa concentrazione sierica), FA placentare e simil-placentare (in gravidanza, prodotte dalla placenta). Un incremento della fosfatasi alcalina si riscontra, oltre che nel danno colestatico, anche in condizioni fisiologiche, quali l’accrescimento e la gravidanza, o in caso di iperattività osteoblastica (Morbo di Paget, iperparatiroidismo, avitaminosi D, metastasi osteoblastiche).
Gamma-glutamiltraspeptidasi
La gamma-glutamiltraspeptidasi (GGT) è un enzima che appartiene alla classe delle transferasi ed è presente in grande quantità nel fegato e nell’epitelio tubulare renale, tuttavia la GGT sierica sembra originare principalmente dal sistema epatobiliare. La GGT è il più sensibile degli enzimi epatici, ma è anche uno dei meno specifici. Un aumento delle GGT, associato ad un incremento della fosfatasi alcalina, si correla a sindrome colestatica. Essendo la GGT un enzima di induzione, un suo incremento si riscontra anche in caso di somministrazione di sostanze che inducono aumento dell’attività disintossicante del fegato, ad esempio alcuni farmaci (antiepilettici e contraccettivi orali) e l’alcool.
Infatti, un aumento isolato della GGT si osserva in soggetti alcolisti, anche in assenza di un’epatopatia. È inoltre frequente riscontrare il reperto di incremento isolato delle GGT nella steatosi epatica non alcolica (NAFLD).
Bilirubina
La bilirubina è un prodotto catabolico del metabolismo dell’emoglobina da parte del sistema reticoloendoteliale. La degradazione dell’eme porta alla formazione di bilirubina non coniugata che viene trasportata nel fegato dove la UDP-glucuronil-transferasi epatica coniuga la bilirubina non coniugata (non solubile) con l’acido glicuronico (bilirubina coniugata, idro-solubile) e poi la secerne nella bile. Un aumento della bilirubina coniugata (o diretta) si ha in caso di ostruzione biliare o di malattie colestatiche autoimmuni. La bilirubina non coniugata (o indiretta) può invece crescere o per aumento della produzione o per ridotta captazione epatica dei prodotti dell’emoglobina. Cause comuni di incremento della bilirubina indiretta sono la sindrome di Gilbert, l’emolisi, l’eritropoiesi inefficace. Frequente è anche un aumento misto della bilirubina che si verifica nella cirrosi o nel danno epatico acuto.
Indici di funzionalità epatica
Tra le più importanti funzioni epatiche bisogna ricordare la sintesi di proteine plasmatiche, quali l’albumina, le alfa e beta globuline, i fattori della coagulazione e alcune frazioni del complemento. L’albumina e il tempo di protrombina (tempo di Quick, PT) sono i principali indicatori di funzionalità epatica. L’albumina è la proteina più abbondante della frazione sieroproteica, rappresenta il 55- 64% delle proteine plasmatiche totali e le sue funzioni principali sono il mantenimento della pressione osmotica del sangue e il trasporto di acidi grassi, ormoni e farmaci. Fra le cause di una sua diminuzione vi è un deficit di sintesi epatica. Il PT è correlato alla via estrinseca della coagulazione. Valori aumentati di PT si riscontrano sia nelle patologie colestatiche, per un deficit dell’assorbimento della vitamina K, sia nelle epatopatie, per un deficit di sintesi.
Alfafetoproteina
Alfafetoproteina (AFP) è un marcatore di replicazione delle cellule epatiche ed è aumentato nei pazienti affetti da epatocarcinoma (HCC). In realtà il monitoraggio dell’AFP non è indicato nello screening dell’HCC ma solo nel determinare la prognosi dei pazienti con HCC già nota.
Esami strumentali
Gli esami strumentali sono fondamentali per la diagnosi e il follow up delle malattie epatiche.
Ecografia
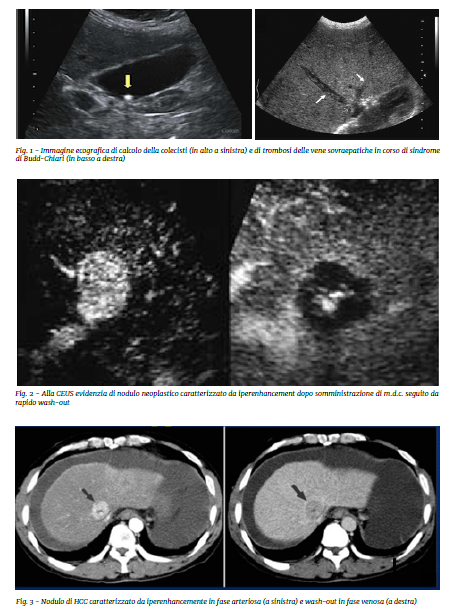
L’ecografia (Fig.1) è molto utile nel sospetto di patologia epatobiliare in quanto dà indicazioni circa la morfologia epatica (dimensioni, ipertrofia del lobo caudato, caratteristiche ecostrutturali, superficie e margini epatici), la presenza di lesioni focali e di segni di ipertensione portale, oltre che valutazione della patologia biliare (ispessimento delle pareti della colecisti, litiasi colecisti e coledocolitiasi).
Principali segni di ipertensione portale sono il calibro dei vasi del sistema venosoportale e la loro espansibilità con la cinetica respiratoria, l’evidenza di circoli collaterali, l’eventuale splenomegalia e versamento ascitico.
L’ecografia con associato studio doppler dei vasi permette inoltre di effettuare una valutazione emodinamica del flusso portale sia qualitativa (presenza e direzione del flusso portale e pervietà e calibro delle vene sovraepatiche) che quantitativa (velocità media portale ed eventuale RI dell’arteria splenica intraparenchimale e delle arterie renali interlobari).
CEUS
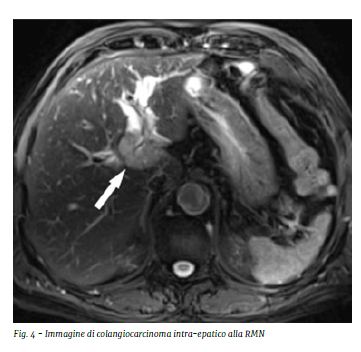
La CEUS (Contrast-Enhanced UltraSonography, Fig.2) rappresenta una metodica capace di unire l’imaging ecografico con l’utilizzo di un mezzo di contrasto endovenoso, composto esclusivamente da bolle d’aria, a distribuzione intravascolare, rendendo così possibile valutare sequenzialmente il comportamento dei vari parenchimi in relazione alla loro vascolarizzazione. La CEUS permette di descrivere accuratamente la vascolarizzazione delle lesioni focali epatiche, permettendo una distinzione tra forme benigne e maligne, pur non consentendo talora una precisa diagnosi di natura. A tal proposito appare sensibile nel caratterizzare angiomi e noduli riferibili a FNH, non altrettanto nel differenziare tra noduli di HCC e colangiocarcinoma (ambedue possono presentare wash-in e wash-out alla CEUS, sebbene con alcune differenze nella distribuzione e nella tempistica). Un’ulteriore utile applicazione della CEUS, sebbene meno suffragata dalla letteratura, è legata al follow-up di lesioni focali epatiche già precedentemente caratterizzate, dati anche il basso costo della metodica, la relativa semplicità di esecuzione e l’assenza di significativi effetti collaterali (reazioni da mdc, esposizione a radiazioni ionizzanti).
Tomografia assiale computerizzata (TC)
La TC addome (Fig.3), corredata dall’utilizzo del mezzo di contrasto iodato, rappresenta un’indagine di secondo livello per lo studio del fegato e dei principali vasi epatici. La metodica si basa sull’analisi computerizzata dell’attenuazione dei raggi X passanti attraverso diverse sezioni corporee. L’utilizzo del mezzo di contrasto iodato, a distribuzione sia intravascolare che interstiziale, si rende necessario per incrementare le differenze di densità tra i tessuti. La cinetica del mezzo di contrasto nei tessuti viene valutata in sequenze cronologicamente successive, dipendenti dalla principale sede di distribuzione dello stesso (arteriosa, portale, venosa, tardiva).
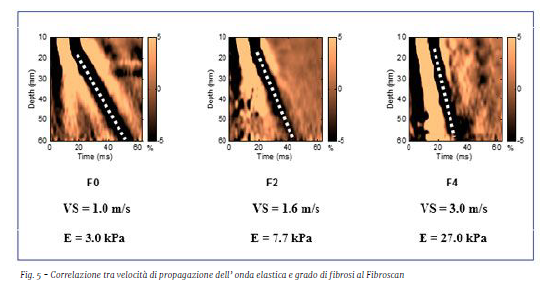
La principale indicazione all’esecuzione della TC addome in epatologia riguarda la valutazione di lesioni focali epatiche sia benigne che maligne, in particolare la diagnosi e la stadiazione dell’epatocarcinoma. L’epatocarcinoma rappresenta forse l’unica neoplasia passibile di diagnosi esclusivamente radiologica, qualora si riscontrino, in un fegato cirrotico, noduli epatici con particolari caratteristiche contrastografiche (wash-in in fase arteriosa e wash-out in fase venosa-portale, per noduli > 1 cm), dipendenti in ultima analisi dalle caratteristiche istologiche tipiche di tale neoplasia.
La completa arterializzazione del parenchima, in assenza di vasi portali, fa sì che il mezzo di contrasto iodato venga assunto molto rapidamente dai noduli di HCC, ed altrettanto rapidamente dismesso. Tale comportamento si traduce nel cosiddetto “wash- in” contrastografico in fase arteriosa (il nodulo appare iperdenso – “più bianco”- rispetto al parenchima circostante), succeduto dal “wash-out” in fase venosa o portale (il nodulo appare ipodenso – “più nero”- rispetto al parenchima circostante).
L’ulteriore importante campo di applicazione della TC addome con mdc è lo studio dell’asse vascolare epatico, in particolare la ricerca e la valutazione delle trombosi splancniche (trombosi della vena porta, trombosi delle vene sovraepatiche- S.di Budd-Chiari), per le quali la TC addome rappresenta la metodica di scelta, superiore alla RMN.
Il principale svantaggio della TC è rappresentato dall’utilizzo di radiazioni ionizzanti.
Risonanza magnetica (RMN)
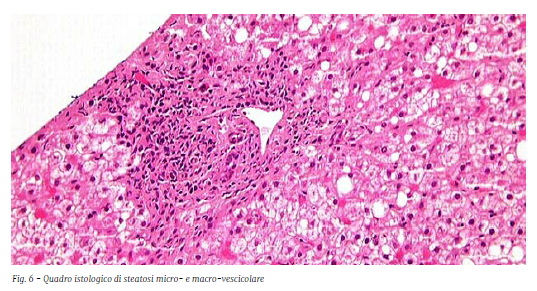
Come la TC addome, anche la RMN (Fig.4 è una metodica radiologica di secondo livello per lo studio del fegato, soprattutto in merito alla valutazione delle lesioni focali epatiche, dove costituisce il “gold standard” tra gli esami di imaging. La RM si basa sulla misura della precessione dello spin di protoni dotati di momento magnetico, quando sottoposti ad un campo magnetico, rilevandone quindi le differenze tra i vari tessuti esaminati, senza utilizzare radiazioni ionizzanti. Anche la RM si avvale dell’utilizzo di mezzi di contrasto al fine di marcare le differenze d’intensità tra i diversi tessuti, potendosi però servire sia di mezzi di contrasto extracellulari come il Gd-DTPA (a distribuzione sia intravascolare che interstiziale), dotati della medesima cinetica dei mdc iodati utilizzati in TC, che di mezzi di contrasto “epatospecifici”, ovvero dotati anche di distribuzione intracellulare (vengono assunti in maniera specifica dagli epatociti “sani”), come il Gd- BOPTA.
La possibilità di utilizzare tali mezzi di contrasto capaci di saggiare anche la corretta funzionalità degli epatociti, e fornire quindi informazioni circa la loro natura benigna o maligna, associata alla possibilità di utilizzare tecniche di caratterizzazione tissutale basate sulle diverse composizioni dei tessuti (es. DWI, sequenze a soppressione del grasso), la RM rappresenta la metodica di scelta per la ricerca e la caratterizzazione delle lesioni focali epatiche, non solo di natura maligna (HCC, colangiocarcinoma), ma anche di natura benigna (angioma, iperplasia nodulare focale, adenoma epatico). Meno accurato rispetto alla TC addome risulta invece lo studio dei vasi epatici.
Fibroscan
L’elastografia epatica, conosciuta anche con il nome commerciale FibroScan (Fig.5), è un sistema di misurazione non invasivo della stiffness del tessuto epatico. L’elastografia prevede l’uso di una sonda ecografica che trasmette un’onda di vibrazione di media ampiezza e bassa frequenza (50 Hz) che si propaga attraverso il fegato, consentendo di valutarne l’elasticità, espressa in kPa. Più il fegato è fibrotico, maggiore è la velocità di propagazione dell’onda. Il valore medio della liver stiffness nel paziente sano è di circa 5.3 kPa, senza che vi siano differenza di età; mentre in relazione al sesso si evidenzia come le donne abbiano mediamente livelli significativamente più bassi. Le stime di elasticità variano da 3 a 75 kPa che corrispondono ad una velocità di propagazione che varia da 1 a 5 m/s. Il risultato è altamente riproducibile e può essere ripetuto nel tempo, permettendo quindi il monitoraggio in modo non invasivo del grado di fibrosi del tessuto epatico nei soggetti affetti da malattie croniche del fegato. Tale test ha inoltre il vantaggio di non procurare dolore e di essere veloce e non invasivo, come potrebbe invece essere la biopsia epatica. Vi sono fattori che possono influenzare l’affidabilità di questo strumento quali il grado di infiammazione epatica (elevazione delle transaminasi) e lo spessore del pannicolo adiposo del paziente analizzato, in quanto il tessuto adiposo attenua sia l’onda elastica che gli ultrasuoni, falsando i risultati ottenuti. Nella pratica clinica quando si interpreta il risultato bisogna tener conto di due parametri: la IQR (variabilità delle misurazioni effettuate) che non deve superare il 30% rispetto alla mediana ed il “success rate” (numero delle misurazioni utili) che deve essere almeno pari al 60% rispetto al numero totale delle acquisizioni svolte.
Biopsia epatica
La biopsia epatica (Fig.6) rappresenta il metodo migliore per la diagnosi delle malattie epatiche acute e croniche ed è generalmente l’ultimo stadio dell’iter diagnostico delle malattie epatiche. Nella maggior parte dei casi permette di formulare una diagnosi di certezza e di chiarire eventuali dubbi sull’etiologia e sulla severità della epatopatia. Può essere, inoltre, utilizzata per valutare l’efficacia di terapie specifiche. La biopsia epatica consiste nel prelievo di un frustolo di tessuto epatico allo scopo di eseguire una valutazione istologica. Può essere eseguita per via percutanea (sottocostale o transcostale) eco assisitita o ecoguidata, ecoendoscopica o direttamente durante un intervento chirurgico addominale. È generalmente una procedura sicura, ma, essendo invasiva, comporta un rischio intrinseco di complicanze quali l’emoperitoneo, la peritonite biliare, le infezioni, l’emotorace, lo pneumotorace, la pleurite, l’ematoma intraepatico e la puntura di altri organi. Attualmente le complicanze sono drasticamente ridotte di numero e di gravità per l’introduzione della guida ecografica e di nuovi aghi di minore calibro e meno traumatici. La remota possibilità di insorgenza di complicanze è, inoltre, da mettere in rapporto all’esperienza dell’operatore.