Fabiola Olivieri *

Prof.ssa Fabiola Olivieri
*Department of Clinical and Molecular Sciences, Università Politecnica delle Marche, Ancona, Italy.
*Center of Clinical Pathology and Innovative Therapy, IRCCS INRCA, Ancona, Italy
La grande variabilità individuale nella presentazione dei sintomi indotti dall’infezione del virus SARS-CoV-2, responsabile della patologia umana nota con il nome di COVID-19, rappresenta una delle principali sfide dal punto di vista sia biologico che clinico, stimolando quindi lo studio dei meccanismi patogenetici che sottendono lo sviluppo ed il decorso di tale patologia. La comparsa della sintomatologia e degli esiti più severi da COVID-19 sembra dipendere da una complessa interazione fra il make-up genetico individuale e numerosi fattori che possono essere genericamente definiti “ambientali”, o con un termine più appropriato “epigenetici”, molti dei quali sono coinvolti nella modulazione della funzionalità del sistema immunitario: tale interazione condiziona la suscettibilità individuale a sviluppare non solo patologie infettive ma anche le più comuni patologie età-associate, quali malattie cardiovascolari, diabete di tipo 2, malattie neurodegenerative e tumori (1, 2, 3).
I pazienti che sviluppano le forme più severe di COVID-19 si caratterizzano per la comparsa di una intensa risposta infiammatoria, spesso associata a fenomeni di trombosi e coagulazione intravasale disseminata, non solo a livello polmonare ma anche in altri distretti, tale per cui può essere definita una risposta infiammatoria sistemica.
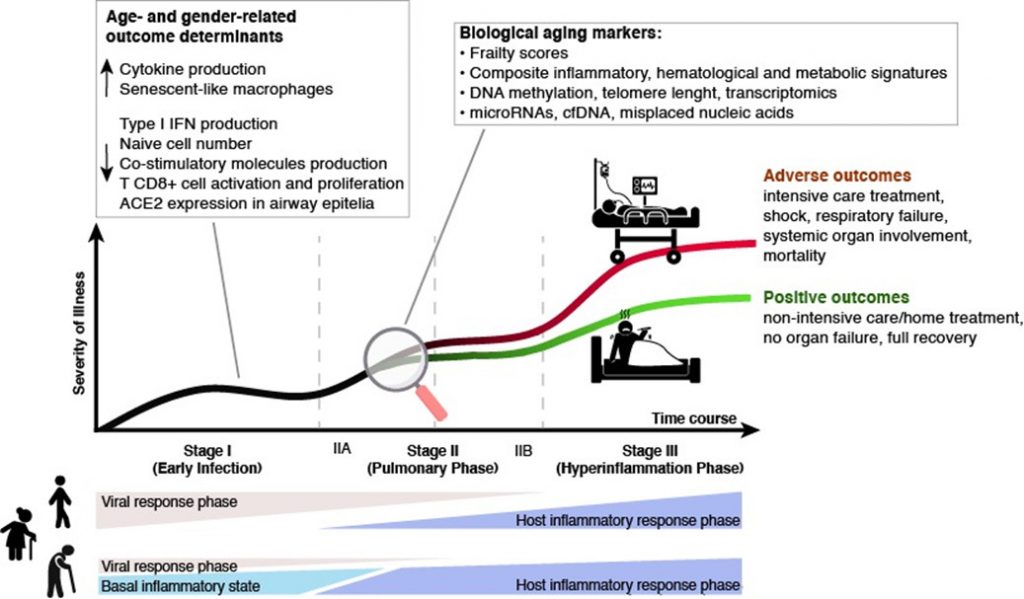
Circa 20 anni fa, siamo stati i primi ricercatori a descrivere all’interno di una ipotesi sostanziata da evidenze epidemiologiche e sperimentali, come l’aumento di uno stato infiammatorio sistemico, di baso grado ma cronico, si associasse all’invecchiamento umano e ne condizionasse il mantenimento di un buono stato di salute: definimmo tale fenomeno “inflammaging” e da allora questo termine è entrato a far parte del dizionario scientifico (4, 5). Basandoci su questa nostra expertise, non è stato difficile ipotizzare che il livello individuale di inflammaging potesse essere considerato non solo un fattore di rischio per lo sviluppo delle più comuni patologie età-associate, ma anche per gli esiti più severi della patologia COVID-19 (Figura 1).
Le similitudini più stringenti fra i meccanismi molecolari coinvolti nell’aumento dell’inflammaging e nella comparsa di esiti severi da COVID-19 possono essere riassunte come segue:
1) iperattivazione dell’immunità innata, soprattutto delle principali cellule dell’immunità innata quali monociti/macrofagi e neutrofili, con aumentata produzione di citochine infiammatorie quali l’IL-6;
2) attivazione dei meccanismi di risposta dell’immunità innata, con particolare riferimento al fenomeno noto come ”Neutrophil extracellular traps (NETs)”;
3) aumentata produzione dei mediatori molecolari coinvolti sia nell’attivazione dell’infiammazione che della coagulazione, quali bradichinina e fattore tissutale;
4) aumentato numero di cellule con fenotipo senescente, e infine 5) alterazioni dei livelli di specifici non coding RNA (in particolare di microRNAs) capaci di modulare i pathways infiammatori, e per questo da noi definiti inflammamiRs, quali ad esempio il miR-146a (3, 6).
Riguardo al ruolo svolto dalle cellule senescenti nel propagare l’inflammaging e nel contribuire a determinare i quadri severi da COVID-19, va ricordato che l’acquisizione di un fenotipo senescente è in grado di trasformare le varie tipologie cellulari in cellule pro-infiammatorie, e questo sembrerebbe valere non solo per le cellule del sistema immunitario (macrofagi, neutrofili e linfociti T), ma anche per cellule endoteliali, fibroblasti e cellule adipose (7, 8).
Intorno alla metà degli anni 2000, il fenomeno della senescenza cellulare era considerato prevalentemente come una strategia messa in atto per arrestare lo sviluppo dei tumori: quando una cellula subisce danni estesi al DNA la divisione cellulare si arresta riducendo le probabilità che si accumulino mutazioni nella progenie cellulare. Nel 2008 però, diversi gruppi di ricerca dimostrarono come le cellule senescenti siano in grado di rilasciare un secretoma (SASP) – contenente citochine, fattori di crescita, proteasi – capace di influenzare la funzionalità delle cellule vicine e stimolare l’infiammazione. Abbiamo di recente dimostrato come anche le vescicole extracellulari debbano essere considerate a tutti gli effetti componenti del secretoma SASP, in quanto rilasciate in maggior quantità da cellule senescenti e capaci di modificare il comportamento biologico delle cellule circostanti (9). Il secretoma delle cellule senescenti tende purtroppo a propagare la senescenza nelle cellule più giovani, alimentando un circolo vizioso che perpetua nel tempo il quadro infiammatorio sistemico. In un tessuto giovane e sano, la SASP acquisisce il significato di un efficiente meccanismo di segnalazione che attira le cellule immunitarie deputate alla clearance delle cellule senescenti, per favorire i fenomeni di rigenerazione e riparo. Tuttavia, con l’invecchiamento dell’organismo, le cellule senescenti cominciano ad accumularsi, soprattutto in pazienti affetti dalle principali patologie età-associate. In questa situazione, il fenotipo SASP anziché promuovere la clearance delle cellule senescenti, concorre ad alimentare l’inflammaging, e in questo contesto potrebbe giocare un ruolo importante anche nel promuovere la patogenesi del COVID-19.
Recenti evidenze suggeriscono come la deriva proinfiammatoria/procoagulante che si osserva nei pazienti affetti da COVID-19 possa essere associata ad un significativo aumento dei livelli di IL-6 in circolo; tale fenomeno è noto sia ai gerontologi che ai geriatri, in quanto livelli aumentati di IL-6 circolante si osservano soprattutto negli anziani e si associano ad aumentato rischio di malattia, disabilità e mortalità. La IL-6 ad oggi è il principale biomarcatore circolante di inflammaging, e i microRNA che modulano la sua sintesi, sia direttamente che indirettamente, quali ad esempio il miR-146a ed il miR-21 sono da considerarsi quali nuovi biomarcatori di inflammaging (10).
Per la cura dei pazienti COVID-19 è stata in effetti proposta la somministrazione di farmaci capaci di bloccare gli effetti biologici dell’IL-6. In questo contesto, abbiamo condotto uno studio pionieristico sulla modulazione degli inflammamiRs in pazienti COVID-19 trattati con farmaci anti IL-6 (quali il Tocilizumab), dimostrando per la prima volta come i livelli di miR-146a circolante fossero in grado di predire l’efficacia della risposta al trattamento (11).
Stiamo al momento indagando su altri inflammamiRs per valutarne la rilevanza clinica quali biomarcatori diagnostico/prognostici nei pazienti affetti da COVID-19.
Concludendo, la nostra decennale expertise sull’inflammaging e sui marcatori circolanti di questo fenomeno, ci consentono di suggerire alcuni meccanismi che potrebbero essere coinvolti nella patogenesi del COVID-19, e di proporre i marcatori circolanti di inflammaging quali nuovi potenziali biomarcatori che potrebbero, se non certo sostituire, almeno affiancare la diagnostica clinica nella complessa gestione del paziente affetto da COVID-19.
Bibliografia essenziale
1. Prattichizzo, F., Sabbatinelli, J., de Candia, P., Olivieri, F., Ceriello, A. Tackling the pillars of ageing to fight COVID-19 The Lancet Healthy Longevity, 2021, 2(4), pp. e191
2. Prattichizzo, F., Bonafè, M., Giuliani, A., …Sabbatinelli, J., Olivieri, F. Response to: Letter to the Editor on “Bonafè M, Prattichizzo F, Giuliani A, Storci G, Sabbatinelli J, Olivieri F. Inflamm-aging: Why older men are the most susceptible to SARS-CoV-2 complicated outcomes. Cytokine Growth Factor Rev” by Eugenia Quiros-Roldan, Giorgio Biasiotto and Isabella Zanella. Cytokine and Growth Factor Reviews, 2021, 58, pp. 141–143
3. Bonafè, M., Prattichizzo, F., Giuliani, A., …Sabbatinelli, J., Olivieri, F. Inflamm-aging: Why older men are the most susceptible to SARS-CoV-2 complicated outcomes. Cytokine and Growth Factor Reviews, 2020, 53, pp. 33–37
4. Franceschi C, Bonafè M, Valensin S, Olivieri F, De Luca M, Ottaviani E, De Benedictis G. Inflamm-aging. An evolutionary perspective on immunosenescence. Ann N Y Acad Sci. 2000 Jun;908:244-54. doi: 10.1111/j.1749-6632.2000.tb06651.x.
5. Fulop T, Witkowski JM, Olivieri F, Larbi A. The integration of inflammaging in age-related diseases. Semin Immunol. 2018 Dec;40:17-35. doi: 10.1016/j.smim.2018.09.003.
6. Storci, G., Bonifazi, F., Garagnani, P., Olivieri, F., Bonafè, M. The role of extracellular DNA in COVID-19: Clues from inflamm-aging. Ageing Research Reviews, 2021, 66, 101234
7. Sabbatinelli J, Prattichizzo F, Olivieri F, Procopio AD, Rippo MR, Giuliani A. Where Metabolism Meets Senescence: Focus on Endothelial Cells. Front Physiol. 2019 Dec 18;10:1523. doi: 10.3389/fphys.2019.01523. eCollection 2019.
8. Zuccolo E, Badi I, Scavello F, Gambuzza I, Mancinelli L, Macrì F, Tedesco CC, Veglia F, Bonfigli AR, Olivieri F, Raucci A. The microRNA-34a-Induced Senescence-Associated Secretory Phenotype (SASP) Favors Vascular Smooth Muscle Cells Calcification. Int J Mol Sci. 2020 Jun 23;21(12):4454. doi: 10.3390/ijms21124454.
9. Mensà E, Guescini M, Giuliani A, Bacalini MG, Ramini D, Corleone G, Ferracin M, Fulgenzi G, Graciotti L, Prattichizzo F, Sorci L, Battistelli M, Monsurrò V, Bonfigli AR, Cardelli M, Recchioni R, Marcheselli F, Latini S, Maggio S, Fanelli M, Amatori S, Storci G, Ceriello A, Stocchi V, De Luca M, Magnani L, Rippo MR, Procopio AD, Sala C, Budimir I, Bassi C, Negrini M, Garagnani P, Franceschi C, Sabbatinelli J, Bonafè M, Olivieri F. Small extracellular vesicles deliver miR-21 and miR-217 as pro-senescence effectors to endothelial cells. J Extracell Vesicles. 2020 Feb 18;9(1):1725285. doi: 10.1080/20013078.2020.1725285. eCollection 2020.
10. Olivieri F, Prattichizzo F, Giuliani A, Matacchione G, Rippo MR, Sabbatinelli J, Bonafè M. miR-21 and miR-146a: the microRNAs of inflamm-aging and age-related diseases. Aging Research Revie (in press)
11. Sabbatinelli, J., Giuliani, A., Matacchione, G., …Bonafè, M., Olivieri, F. Decreased serum levels of the inflammaging marker miR-146a are associated with non-clinical response to tocilizumab in COVID-19 patients. Mech Ageing Dev. 2021 Jan;193:111413. doi: 10.1016/j.mad.2020.111413
Figura 1. L’inflammaging quale meccanismo patogenetico che potrebbe concorrere allo sviluppo dei quadri più severi da COVID-19, osservabili soprattutto negli anziani fragili. In questo contesto, i biomarcatori di inflammaging si configurano quali potenziali markers diagnostico/prognostici per COVID-19.