Laura Buratti
Dipartimento di Medicina Sperimentale e Clinica, Sezione Clinica Neurologica Facoltà di Medicina e Chirurgia, Università Politecnica delle Marche
Le benzodiazepine sono tra i farmaci più prescritti a livello mondiale e sono caratterizzate da diverse attività far– macologiche: anticonvulsionante, miorilassante, ansiolitica, ipnoinducente. La loro efficacia è indubbia, ma possono determinare l’insorgenza di effetti indesiderati, soprattutto negli anziani. Nonostante largamente utilizzate, è scarsamente conosciuta l’esatta tempistica del loro utilizzo sia tra i pazienti sia tra i medici, generando frequentemente fenomeni di dipendenza e tolleranza. La dipendenza da benzodiazepine è, infatti, la più tipica dipendenza generata da prescrizione medica ed è un problema diffuso, rilevante, misconosciuto. E’ quindi doveroso da parte del medico conoscere il loro corretto utilizzo e le modalità di trattamento dell’abuso per evitare complicanze.
Le benzodiazepine (BDZ) sono molecole che agiscono a livello del sistema nervoso centrale potenziando la trasmissione GA- BA-ergica (GABA-A); l’interazione delle BDZ con il proprio recettore facilita il legame del GABA con il suo recettore, producendo l’apertura dei canali del cloro nel neurone postsinaptico con un effetto inibitorio sull’attività neuronale. Le BDZ interagiscono con siti di legame specifici (siti modulatori) che sono parte integrante del complesso macromolecolare del recettore del GABA, neutrotrasmettitore inibitorio più importante tra quelli presenti nel cervello dei mammiferi.
Il recettore GABA-A è un pentamero costituito da due subunità α, due subunità β e una subunità λ, disposte intorno al canale del cloro.
Esistono diversi sottotipi delle subunità che costituiscono il recettore GABA-A generando diversi sottotipi recettoriali localizzati in diverse aree cerebrali; le BZD legano un sito tra le subunità α e γ, riconoscono le subunità α1, α2, α3 e α5 ma non le subunità α4 e α6 (Figure 1, 2)¹–²
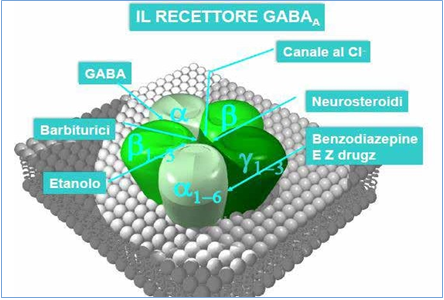
Figura 1 – GABA-A è un pentamero costituito da due subunità α, due subunità β e una subunità γ. Le BZD legano un sito tra le subunità α e γ e sono in grado di modulare la conduttanza al cloro (ulteriore apertura del canale) attraverso un meccanismo di modulazione allosterica. Esistono diversi sottotipi delle subunità che costituiscono il recettore GABAA generando diversi sottotipi recettoriali
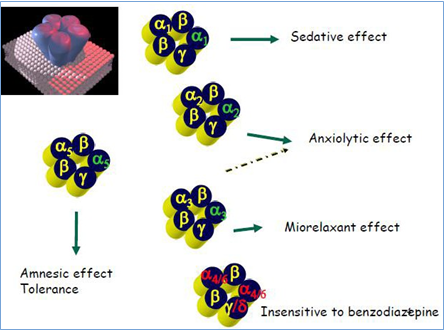
Figura 2 – Le BZD riconoscono le subunità α1 , α2 , α3 e α5 ma non le subunità α4 e α6
Le attività farmacologiche delle BDZ sono sostanzialmente: anticonvulsionante, miorilassante; ansiolitica, ipnoinducente (Tab. 1).
| Effetti farmacologici BDZ | Effetti collaterali BDZ | Sindrome astinenziale da BDZ |
| anticonvulsionante, miorilassante, ansiolitico, ipnoinducente. |
sedazione, sonnolenza, amnesia, atassia, disartria, astenia e rilassamento muscolare, incoordinazione motoria motoria (causa spesso di cadute negli anziani) e riduzione delle performances cognitive (quadri pseudodemenziali con rischio di errore diagnostico) e psicomotorie. |
sudorazione, tachicardia, ansia, agitazione, irritabilità, tremore, insonnia, nausea e vomito, deflessione del tono dell’umore, tensione muscolare, a volte allucinazioni visive, tattili e uditive, crisi comiziali |
Tabella 1 – Effetti farmacologici, collaterali, astinenziali delle BDZ
I recettori BDZ 1 o Omega 1 presenti prevalentemente nel cervelletto e corteccia cerebrale sono implicati nell’azione ansiolitica/ iponinducente, i recettori BDZ 2 o Omega 2 prevalentemente localizzati nel midollo spinale, striato e nell’ippocampo sono associati alle subunità α2, α3, α5 sono implicati nell’azione miorilassante e anche cognitiva.
Le BDZ di seconda generazione (Z-drugs: zolpidem zopiclone..) esercitano la loro azione su Ome- ga 1, sono selettive per i recettori GABA-A che contengono subu- nità a1, vengono utilizzate come ipnoinducenti e sono sostanzial- mente prive di attività ansiolitica, miorilassante e anticonvulsionante (Tab.2)³-⁵
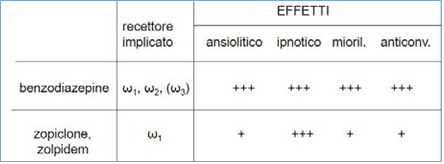
Tabella 2 – Azione selettiva delle Z-drugs rispetto alle BDZ di prima generazione
Le principali indicazioni terapeutiche delle BDZ sono rappresentate da insonnia, stati di ansia, condizioni di spasticità, contrattura e/o rigidità muscolare. Le BDZ si classificano in base alla loro diversa emivita di eliminazione: ultrabreve (2-5 ore), breve (6-24 ore) medio-lunga (oltre 24 ore).
Benchè siano molecole caratterizzate da elevata maneggevolezza, le BDZ possono determinare l’in- sorgenza di effetti indesiderati. Tra questi si segnalano: sedazione, amnesia, atassia, disartria, astenia e rilassamento muscolare, incoordinazione motoria (causa spesso di cadute negli anziani) e riduzione delle performances cognitive (quadri pseudodemenziali con rischio di errore diagnostico) e psicomotorie. Negli anziani è frequente anche la comparsa di effetti paradossi caratterizzati da alteraassociati alla subunità α1 e sono
zioni comportamentali, aggressività, agitazione psicomotoria(nel paziente anziano: decremento della funzione metabolica epatica, soprattutto per ciò che concerne i processi ossidativi con conseguente possibilità di fenomeni di accumulo in caso di somministrazioni ripetute) (Tab. 1).
Gli effetti indesiderati delle BDZ sono spesso una estensione delle loro attività farmacologiche⁶. Sono tra i farmaci più prescritti a livello mondiale; nel nostro Paese, per intenderci, ne fa uso un adulto su dieci, una percentuale che sale fino ad uno su quattro nella fascia di età sopra i 65 anni, con conseguenze importanti. Infatti, se è vero che le BDZ si sono mostrate efficaci nel curare disturbi di ansia, insonnia, depressione ansiosa è altrettanto vero che l’uso prolungato espone al rischio di sviluppare dipendenza e tolleranza.
Tutte le sostanze d’abuso inducono un effetto sul sistema neuronale del circuito della gratificazione (circuito dopaminergio sistema mesolimbico-mesocorticale) L’esposizione cronica a qualsiasi sostanza d’abuso porta ad una riduzione nella risposta del circuito di rinforzo della dopamina; l’uso ripetuto di sostanze psicotrope altera la risposta agli stimoli naturali, rendendoli meno piacevoli rispetto a quanto lo erano precedentemente.
La dipendenza è una malattia cro- nica recidivante caratterizzata da ricerca e da uso compulsivo della sostanza d’abuso (craving) e da cambiamenti neurochimici e mole- colari nel cervello.
Dipendenza fisica: fenomeno associato alla tolleranza, caratterizzato da comparsa di sintomi fisici (sintomi da astinenza) che spingono il soggetto ad assumere la sostanza al fine di mantenere la normale funzionalità fisica. Dipendenza psichica: si manifesta quando una sostanza agisce sul circuito della gratificazione. La sensazione di piacere che scaturisce dall’assunzione porta al desiderio di continuare ad assumerla.
Tolleranza: è un fenomeno fisiologico che spinge la persona ad assumere sempre maggiore quantità di sostanza per ottenere lo stesso effetto (Tolleranza farmacodinamica: assunzione di maggiori quantità della sostanza a causa di una riduzione della capacità di risposta dei recettori desensibilizzazione e dei processi fisiologici intracellulari). In relazione al rischio di sviluppare dipendenza e tolleranza (assuefazione) anche in tempi brevi, l’uso delle BDZ è da tempo raccomandato per un periodo limitato intorno alle quattro settimane.
Le BDZ sono una classe di farmaci adatta a terapie brevi e non a terapie di mantenimento a lungo termine: nel caso di ansia cronica, la terapia di lunga durata deve essere gestita da farmaci antidepressivi, senza trascurare l’importanza del- la psicoterapia. In tal senso, è consigliabile l’uso di BDZ nella fase iniziale di trattamento, per coprire la fase di latenza di un antidepressivo.
Vi è invece una tacita accettazione, da parte di medici e pazienti, dell’uso a lungo termine delle benzodiazepine. Si assiste quindi a un numero sempre maggiore di pazienti che fanno un uso prolungato senza interruzioni del trattamento a dosi terapeutiche e pazienti che assumono BDZ a dosi extra-terapeutiche per fenomeni di tolleranza.
Un’altra situazione è quella dell’a- buso saltuario di dosi inappropria- te di BDZ (“sbornia di BDZ”). Tale modalità coinvolge soprattutto i soggetti affetti da dipendenza da sostanze illecite ed alcol o i sogget- ti con disturbi di personalità. Per l’uso tossicomanico il più utilizza- to è il lormetazepam (Minias); per i noti rischi di abuso il Minias gtt è disponibile solo in Italia e Spagna. La dipendenza da BDZ ad alte dosi presenta un impatto economico notevole.
Parlando in termini concreti si vedono pazienti che arrivano ad usare 6 flaconi di Minias (3600 gtt) al giorno, circa 1250 euro al mese! (8). Oltre al lormetazepm (Minias) anche altre BDZ sono facilmene abusate: lorazepam (Tavor), triazolam (Halcion), alprazolam (Xanax), zolpidem (Stilnox).
La dipendenza da BDZ è la più ti- pica dipendenza iatrogena, ossia originata da prescrizione medica. I medici raramente avvertono il paziente che il trattamento deve essere molto breve, oppure episo- dico, per evitare il rischio di dipendenza e tolleranza (è scritto anche sul depliant illustrativo).
Questo cosa comporta? Che la paziente X prende per un mese BDZ per curare l’ansia e negli anni successivi crede di fare la stessa cosa, ma in realtà, senza saperlo, continua a prenderle solo per evitare la sindrome di astinenza da queste causata.
La paziente X non sa (e anche il suo medico) che, dopo 30-40 gg di uso regolare le BDZ cessano ogni effetto terapeutico (per una modifica dei recettori di membrana). Quindi se dopo tre mesi la paziente X sta bene con il farmaco, sarebbe stata bene anche non lo avesse mai assunto. Le BDZ danno dipendenza ed i sintomi di astinenza non vengono riconosciuti perché sono di lunga durata ed identici ai disturbi iniziali.
La sindrome di astinenza è caratterizzata da una serie di segni e sintomi tipici che cominciano a manifestarsi entro qualche ora o qualche giorno dalla sospensione del farmaco. In particolare, sudo- razione, tachicardia, compaiono ansia, agitazione, irritabilità, tre- more, insonnia, nausea e vomito, deflessione del tono dell’umore, tensione muscolare, a volte allucinazioni visive, tattili e uditive. Il sintomo più temibile è rappresentato dalle crisi convulsive generalizzate, potenzialmente letali in caso di occorrenza durante guida⁹ (Tab 1).
I sintomi astinenziali possono durare a lungo mettendo a dura prova chi cerca di smettere. I tradizionali programmi di scalo, raccomandati in intervalli temporali tra le 4 e le 18 settimane, perdono generalmente di efficacia passando dal trattamento da uso cronico di dosi terapeutiche alle dosi extraterapeutiche di BDZ10. Le principali condizioni di abuso sono così riassumibili (Tab. 3):
Tabella 3 – Spettro degli usi sconsiderati di BDZ
Abuso acuto del tossicomane, di pendenza da basse dosi, dipendenza da alte dosi. Da alcuni anni l’Unità di Degenza di Medicina delle Dipendenze di Verona (una delle poche anche livello internazionale) (Lugoboni e coll.) applica il trattamento con flumazenil in infusione lenta nei casi di abuso cronico di alte dosi di BDZ. Il trattamento permette di sospendere in tempi rapidi (7-8 giorni) dosi molto alte di BDZ in modo ben tollerato e con scarsi effetti collaterali. Diviene sempre più importante conoscere la corretta gestione della dipendenza da BDZ.
Esistono ad oggi tre metodi di trattamento:
Trattamento della dipendenza da BDZ
1: riduzione scalare della BDZ usata
2: sostituzione con BDZ a lunga durata di azione (preferibile nei dosaggi non troppo elevati)
3: trattamento con antagonista competitivo del sito di legame recettoriale (flumazenil/Anexate) (forme più gravi, dosaggi molto elevati, in ambito ospeda- liero)
- 1 metodo: riduzione scalare del- la BDZ abusata; riduzione molto lenta del farmaco (da un mese a 6-12 mesi a seconda della dose). In teoria logico, nella pratica la lun- ghezza del percorso, la comparsa di sindrome astinenziale, l’abuso compensatorio, fanno fallire il progetto
- 2 metodo: sostituzione con una BDZ a lunga di azione: clonaze- pam (Rivotril): più efficace nella dipendenza da dosaggi non troppo elevati (es. 6-10 mg alprazolam). Passare da lormetazepam, zolpidem, alprazolam al clonazepam ha lo stesso razionale del passare dall’eroina al metadone. Scalare il clonazepam è poi più semplice che scalare la BDZ a breve emivita. Esiste però il non remoto rischio di utilizzo cronico del clonazepam, così come succede con il metadone. Il clonazepam viene scelto per:
-lunga emivita (livelli ematici stabili); picco ematico più lento rispetto alle altre BDZ a lunga emivita (minor rischio di abuso rispetto ad altre BDZ); forte legame recettoria- le (meno sensibilità verso la BDZ d’abuso). - 3 metodo: trattamento con anta- gonista competitivo del recettore BDZ: Flumazenil (Anexate). Una settimana-dieci giorni di rico- vero per la disassuefazione com- pleta. Si utilizza il farmaco infusione lenta con elastomero per sette giorni, previa copertura antiepi- lettica. Il recupero del paziente è in genere rapido e completo, con normale ripristino della funzione dei recettori del GABA11.
Conclusione
l’assunzione per brevi periodi (es. per una insonnia tran- sitoria) che risponderebbe in pieno alle indicazioni previste per questa categoria di farmaci riguarda solo un quinto della popolazione generale. Andrebbe quindi migliorata l’informazione sul corretto utilizzo di questi farmaci. La dipendenza da BDZ, spesso di origine iatrogena, è un problema diffuso, rilevante, misconosciuto e poco e male trattato. In relazione agli argomentati rischi, è di rilevante importanza riconoscerla e trattarla correttamente. Il trattamento ospedaliero è stato promosso dall’Unità di Degenza di Medicina delle Dipendenze di Verona rimane a tutt’oggi poco conosciuto e praticato12-14.
Bibliografia
- Conti et al. Fisiologia Medica. 2010; volume 1; cap. 38: 831-845.
- Nidhi Arora, Prashant Dhi- man, Shubham Kumar, Gurpreet Singh, Vikramdeep Monga. Recent advances in synthesis and medicinal chemistry of benzodiazepines .Bioorg 2020 ;97:103668
- J E Kralic 1, T K O’Buckley, R T Khi- sti, C W Hodge, G E Homanics, A L GABA(A) receptor alpha-1 subunit deletion alters receptor subtype assembly, pharmacological and beha- vioral responses to benzodiazepines and zolpidem Neuropharmacology. 2002 ;43:685-94.
- André S. Pollmann, Andrea L. Mur- phy, Joel C. Bergman, David M. Gar- Deprescribing benzodiazepines and Z-drugs in community-dwelling adults: a scoping review. Pharmacol Toxicol. 2015; 16: 19.
- Jaden Brandt, Christine Leong. Ben- zodiazepines and Z-Drugs: An Upda- ted Review of Major Adverse Outcomes Reported on in Epidemiologic Research Drugs R D. 2017; 17: 493–507.
- Michael Kang , Michael A. Galu- ska , Sassan Ghassemzadeh Benzodia- zepine Toxicit. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publi- shing; 2020 Jan.2020 Jul 1.
- Michael Soyka, Bernau München. Treatment of benzodiazepine depen- dance. Fortschr Neurol Psychiatr. 2019 Apr;87(4):259-270.
-
- Victoria R. Votaw, Rachel Geyer, Maya M. Rieselbach, R. Kathryn McHu- gh.The epidemiology of benzodiazepi- ne misuse: A systematic review. Drug
- Lone Baandrup, Bjørn H Ebdrup, Jesper Ø Rasmussen, Jane Lindschou, Christian Gluud, Birte Y Glenthøj. Pharmacological interventions for ben- zodiazepine discontinuation in chro- nic benzodiazepine users. Cochrane Database Syst 2018 Mar; 2018(3): CD011481. Published online 2018 Mar 15. doi: 10.1002/14651858.CD011481. pub2
- Pedro Mateu-Gelabert, Lauren Jes- sell, Elizabeth Goodbody, Dongah Kim, Krista Gile, Jennifer Teubl, Cassandra Syckes, Kelly Ruggles, Jeffrey Lazar, Sam Friedman, Honoria Guarino. High enhancer, downer, withdrawal helper: Multifunctional nonmedical benzodia- zepine use among young adult opioid users in New York Int J Drug Poli- cy.2017; 46: 17–27.
- Sean David Hood, Amanda Nor- man, Dana Adelle Hince, Jan Krzysztof Melichar, Gary Kenneth Hulse. Ben- zodiazepine dependence and its tre- atment with low dose flumazenil. Br J Clin Pharmacol. 2014 Feb; 77: 285–294. 12.Fatema Tun Naher Sake, Keith Wong, Delwyn J. Bartlett, Bandana Sai- ni. Benzodiazepine usage and patient preference for alternative therapies: A descriptive Health Sci Rep. 2019; 2: e116.
- David S. Kroll, Harry Reyes Nieva, Arthur J. Barsky, Jeffrey A. Linder. Ben- zodiazepines are Prescribed More Fre- quently to Patients Already at Risk for Benzodiazepine-Related Adverse Even- ts in Primary Care. J Gen Intern 2016; 31: 1027–1034.
- F Cosci , G Mansueto , M Faccini , R Casari , F Socio-demographic and clinical characteristics of benzodia- zepine long-term users: Results from a tertiary care center. Compr Psychiatry. 2016; 69: 211-5
